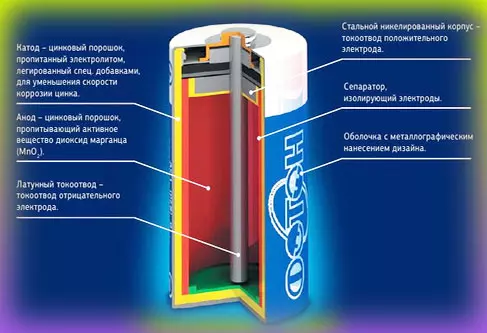
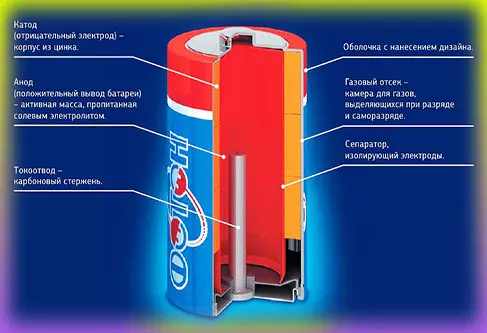
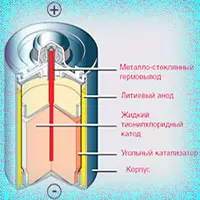
Повседневная жизнь не требует каких-то великих усилий для включения телевизора, калькулятора, для нормальной работы настенных часов, для работы компьютерной мыши и так далее. А все благодаря каким-то батарейкам, которые помогают упростить нашу жизнь, помогают сэкономить наше время. Это понимает каждый здравомыслящий человек, но не каждый задаёт себе вопрос: «как из таких маленьких батареек совершается такой объём работы», «как устроены батарейки»… А, между тем, это физика.
Самые первые прототипы батареек появились ещё в Месопотамии около 2000 лет назад. Состояла она в то время из глиняной вазы, медного и железного стержней, залитыми битумом. Кстати, если такой сосуд залить кислотой (уксусной, серной), то получим напряжение примерно в 1В. Назвали такой прототип «Багдадской батарейкой » в связи с местом, на котором были обнаружены.
Примерно в 1800 году итальянский физик Алессандро Вольта изобрёл батарейку, которой мы и по сей день продолжаем пользоваться. Кстати, кто не знает что такое батарейка, так это источник питания, который вырабатывает электричество под действием химического процесса. То есть батарейка это гальванический элемент, работающий на химической реакции. Так можно объяснить и детям.
Возможно, вам будет интересно: Почему батарейки кислые на вкус?
Видео:БАТАРЕЙКИ. История развития и разновидности.Скачать

 Как работает батарейка
Как работает батарейка
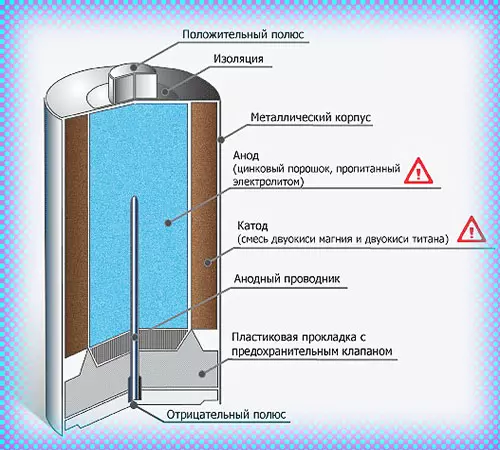
Катоды выполняют функцию восстановителя, т.е. принимают электроны от прибывшего анода. Электролит это среда, в которой перемещаются ионы, которые образуются в процессе химической реакции. В процессе работы батарейки постепенно образовываются новые вещества, а электроды постепенно разрушаются — батарейка садится.
Вот и вся работа батарейки, кстати, все процессы, проходящие в гальваническом элементе, необратимы, то есть заряжать батарейки нельзя. Кратко говоря о работе батарейки: анод — нагрузка — катод — электролит.
Электролит изначально изготовляли в жидком виде, но это неудобно, так как при переворачивании батарейки она просто не работала. Из-за этого электролит стали загущать, превращать его в сухой вид.
Видео:Как работает батарейка?Скачать

 Как устроена батарейка
Как устроена батарейка
Внутри металлического корпуса щелочной ячейки находятся три основных химических вещества: цинк, диоксид марганца и гидроксид калия.
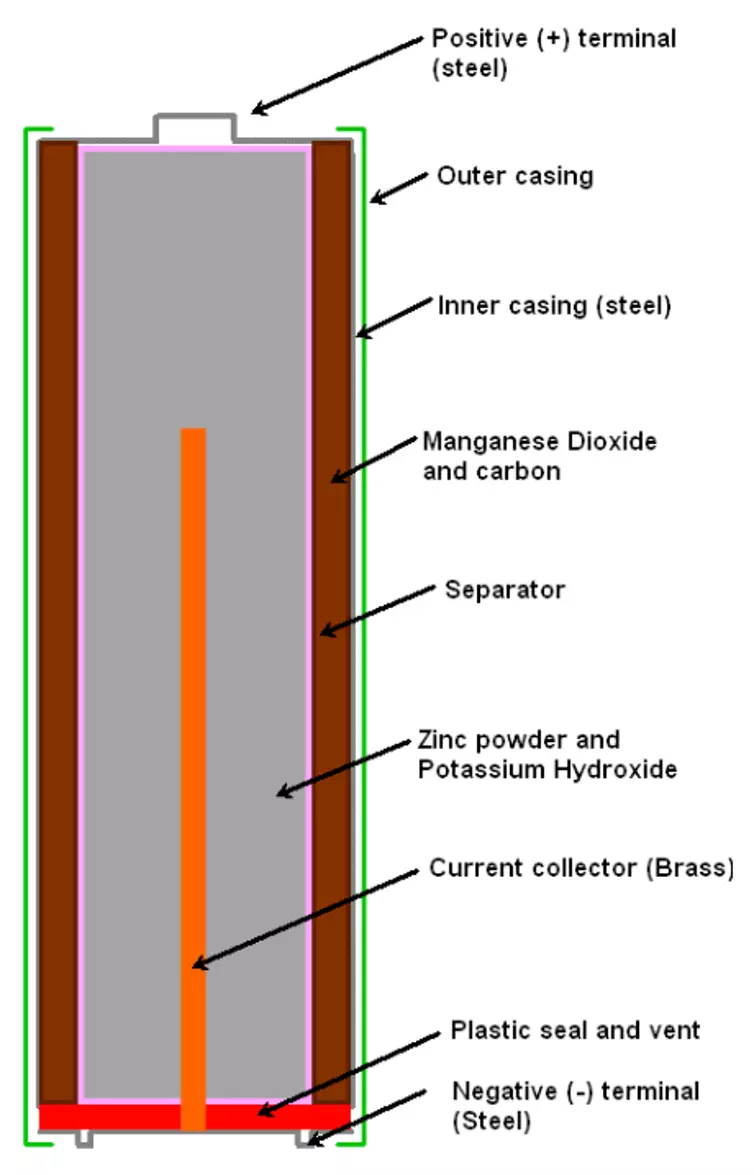
Это может показаться сложным, но способ производства электричества в батарейке на самом деле довольно прост: происходит химическая реакция, которая перемещает крошечные отрицательно заряженные частицы, называемые «электронами», вокруг, чтобы создать электрический ток.
Когда элемент подключен к цепи — например, к лампочке, — цинк внутри реагирует с диоксидом марганца и теряет электроны.
Электроны собираются с помощью металлического стержня внутри ячейки, что позволяет им течь из нижней части ячейки (отрицательный), через провода к лампе (чтобы она загорелась), а затем обратно в верхнюю часть ячейки. (положительный).
Эта реакция производит около 1,5 вольт электроэнергии. Поскольку не так много устройств могут работать при напряжении 1,5 В, очень часто два или четыре элемента используются вместе для увеличения мощности. Таким образом, четыре ячейки, соединенные вместе (конец в конец), дадут шесть вольт.

Когда большая часть цинка прореагировала с диоксидом марганца, мы говорим, что элемент «плоский», что означает, что он больше не может производить электричество. Поскольку химическая реакция, происходящая в щелочных элементах, не может быть легко изменена, это означает, что элемент не может быть перезаряжен.
Но помните, что большинство элементов и батарей можно утилизировать, поэтому убедитесь, что вы тщательно от них избавились.
Видео:Какие бывают батарейки?Скачать

 Обратная реакция
Обратная реакция
Все типы батареек и элементов имеют сходный тип химической реакции, происходящей для выработки электроэнергии.
Но в некоторых типах элементов или батарей химические вещества различны, и реакция может быть обратной. Таким образом, элементы могут быть перезаряжены — так же, как литий-ионные аккумуляторы в автомобилях или смартфонах.

Раньше было гораздо дешевле производить неперезаряжаемые элементы, такие как щелочные элементы, поэтому они использовались очень широко.
Но теперь, когда люди осознали, насколько вредно для окружающей среды просто выбрасывать неперезаряжаемые элементы, а поскольку перезаряжаемые элементы становятся дешевле, мы, вероятно, будем использовать неперезаряжаемые элементы все меньше и меньше в будущем.
Видео:САМАЯ ОПАСНАЯ БАТАРЕЙКА В МИРЕ!Скачать

 Типы батареек
Типы батареек
- Солевые (угольно-цинковые, марганцево-цинковые) батарейки.
Что это такое солевые батарейки
Солевая батарейка изготавливается из пассивного угля и двуокиси марганца, электролит из хлорида аммония и катод из цинка. В перерывах работы элементы питания могут восстанавливаться, т.е. выравнивать локальные неоднородности в композите электролита, вызванных разрядом. Такой процесс немного продлевает срок службы батарейки.
- Алкалиновые (щёлочные) батарейки
Алкалиновые (щелочные) батарейки что это такое
В отличие от солевых батарей у алкалиновой батарейки химический элемент электролита — щелочной. Щёлочные батарейки (алкалин) имеют продолжительный срок хранения, а в процессе эксплуатации напряжение на электродах меняется гораздо меньше, чем у элементов с солевым раствором.
- Литиевые батарейки — li ion
Литиевые батарейки — что это такое?
Самые современные. В отличие от щелочных и солевых батареек, в состав катода входит литий (Li – наивысший отрицательный потенциал), в состав анода — различные материалы. Электролит — органический электролит. В связи с такими элементами литиевые батарейки получили большой срок хранения, большую плотность энергии и различную рабочую температуру.
🔍 Видео
Sony Playstation Portable в 2024 годуСкачать

ЧТО ВНУТРИ БАТАРЕЙКИ и как она работает? ▶️ Часть 1 | COMFYСкачать

Галилео 🔋 Что находится внутри пальчиковой батарейки?Скачать

Жуки - Батарейка.Скачать

Какие батарейки лучше: солевые или щелочные #shortsСкачать

КАК РАБОТАЮТ почти ВЕЧНЫЕ БАТАРЕЙКИСкачать

Как проверить батарейки. 3 способа. Прыгающие батарейки!Скачать

ЗАЧЕМ НУЖНЫ АААА - БАТАРЕЙКИСкачать

РАСПИЛИЛИ БАТАРЕЙКИ! ЧТО ОКАЗАЛОСЬ ВНУТРИ НИХ?Скачать

Какие батарейки работают дольше? (короткая версия)Скачать

Химия из батарейкиСкачать

Батарейки — это ХИТ! Как работают солевые, щелочные и какие батарейки лучше?Скачать

▶ БАТАРЕЙКИ больше НЕ ПОКУПАЮ ! ✔ самодельная БАТАРЕЙКА ИЗ СОДЫ решит все проблемы !Скачать

КАК СДЕЛАТЬ ВЕЧНУЮ БАТАРЕЙКУ - ЭКСПЕРИМЕНТСкачать

Реально ли Сделать БАТАРЕЙКУ ИЗ ГРЯЗИ?Скачать

Включится ли телевизор от батарейки?Скачать



 Как работает батарейка
Как работает батарейка Как устроена батарейка
Как устроена батарейка Обратная реакция
Обратная реакция Типы батареек
Типы батареек